


私たちの体質は一人ひとり異なります。 ある疾患にかかりやすい人とかかりにくい人、同じ薬を飲んでも薬が効きやすい人、効きにくい人、副作用が出る人がいます。 従来の標準的な医療では同じ疾患の患者さんに同じ薬が使用されることが多く、 患者さんによっては望んだ治療効果が得られない場合や副作用が出てしまう場合があります。 このような体質の違いは一人ひとりが持つ遺伝情報の違いによって決まっています。

近年、次世代シークエンサーをはじめとしてゲノム解析技術が大きく進歩し、医療現場でも遺伝情報を活用する動きが盛んになりつつあります。 一人ひとりのゲノムの違いを調べることで、その人が特定の疾患に罹患する可能性や、治療効果、副作用の有無を予測し、 効果的な治療法の選択に繋げられると期待されます。 このように、遺伝情報に基づき個人の体質や病状に合った診断や治療を行うことを『オーダーメイド医療』と呼びます。

当研究チームでは、オーダーメイド医療の実現に向けてバイオバンク・ジャパンと共にゲノムワイド関連解析を中心とした手法により 疾患発症に関連する遺伝的バリアントを同定してきました。 近年では、乳がんや前立腺がんをはじめとするがんを対象として大規模なゲノム解析を実施しています。 乳がんでは、個人のゲノムを調べる遺伝学的検査の結果を踏まえた未発症臓器の予防的切除やPARP阻害剤の投与などが保険適応となっています。 このような遺伝情報に基づく治療や予防法を更に確立するため、複数のがんを対象として発症に関連する遺伝子の探索的解析を行っています。
当研究チームがこれまでに研究対象とした疾患と研究内容をご紹介します。
2013年にアメリカの女優アンジェリーナ・ジョリーさんは、 自身がBRCA1遺伝子の病的バリアント(疾患の発症に繋がる1カ所のゲノム配列の違い)の保有者であり、 それにより乳がんのリスクが他人の10倍以上高くなることから、発症予防のために乳房切除をしたことを公表しました。 このニュースは日本でも話題になり、日本人においてどの遺伝子にどのような頻度で病的バリアントが存在するか、 病的バリアントを持つ人にどのような臨床的特徴があるかを明らかにする必要がありました。 当研究チームでは、疾患群として日本人の乳がん患者さん約7,100名、 対照群としてがん未発症の方約23,000名のゲノム解析を行いました。 その結果、疾患群のうち5.7%はBRCA1、BRCA2遺伝子などの遺伝性腫瘍関連遺伝子に 病的バリアントを持っていることが明らかとなりました。 なお、National Comprehensive Cancer Network が作成した診療ガイドラインでは 11個の遺伝子が遺伝学的検査の対象となっていましたが、 実際に乳がん発症と関連していた遺伝子はBRCA1、BRCA2などの8個で、 残りの3遺伝子は日本人においては乳がん発症との関連は認められませんでした。 また、40歳未満で診断された方のうち15%が病的バリアントを保有しており、 診断年齢が上がるごとにその割合は減少していましたが、 80歳以上で診断された方においても3.2%は病的バリアントを保有していました。 この数値は対照群の約5倍であり、高齢であってもBRCA1、BRCA2遺伝子が発症に影響することが明らかとなりました。 これらの結果は 遺伝性乳癌卵巣癌(HBOC)診療ガイドライン に掲載され、 実際の臨床現場で利用されています。
前立腺がんは年々患者数が増加しており、日本人男性において最も罹患人数が多いがんです。 前立腺がんでは、BRCA1、BRCA2をはじめとする遺伝子上に存在する病的バリアントが発症に寄与することが示唆されていましたが、 乳がんに比べてデータの蓄積が少なく、詳細な関連は明らかにされていませんでした。 そこで当研究チームでは、疾患群として前立腺がん患者さん約7,600名、対照群としてがん未発症の方約12,000名を対象として、 過去に報告されていた病的バリアントが存在する8遺伝子を解析しました。 その結果、BRCA2、ATM、HOXB13遺伝子上の病的バリアントが前立腺がんの発症に関連することが明らかとなりました。 これらの結果は 遺伝性乳癌卵巣癌(HBOC)診療ガイドライン に掲載され、実際の臨床現場で利用されています。
膵がんは、発生率および死亡率が世界的に増加しており、5年生存率が極めて低いがんです。 一部の膵がんは単一の病的バリアントが発症の原因になっていると考えられていましたが、 膵がん患者さんを対象として大規模に病的バリアントを解析した研究は海外を含め2例しか存在せず、 遺伝情報を用いた医療の障壁となっていました。 そこで当研究チームでは、疾患群として膵がん患者さん約1,000名、対照群約としてがん未発症の方約20,000名を対象として 27個の遺伝性腫瘍関連遺伝子を解析し、膵がんの病的バリアントを205個同定しました。 さらに、3つの遺伝子(BRCA1、BRCA2、ATM遺伝子)が膵がんの発症に関連し、 疾患群1,009名のうち5.1%がこれらの遺伝子上に病的バリアントを保有していること、 病的バリアント保有者は胃がんや卵巣がんの家族歴を高頻度で有することを明らかにしました。 これらの結果は 遺伝性乳癌卵巣癌(HBOC)診療ガイドライン に掲載され、実際の臨床現場で利用されています。
腎がんは日本では年間約3万人が発症しているがんです。 また、腎がんは淡明細胞型腎細胞がんと、非淡明細胞型腎細胞がんの二つに分かれ、 それぞれの組織型で予後などに違いがあると言われています。 これまで、腎がんでは原因遺伝子に応じた組織型があることや予後に影響を与えることが明らかになっていますが、 日本人においての情報は多くありませんでした。 そこで、当研究チームは腎がん患者さん約1,500名および対照群としてがん未発症の方約6,000名を対象として、 40個の遺伝子を解析しました。 その結果、淡明細胞型腎細胞がん患者さんでは5個の遺伝子(TP53、CHEK2、BAP1、VHL、PMS2)、 非淡明細胞型腎細胞がん患者さんでは4個の遺伝子(BAP1、FH、TSC1、FLCN)が発症に関連していることがわかり、 組織型によって原因遺伝子が異なることやその臨床的な特徴を明らかにしました。 これらの結果は腎癌のゲノム医療に貢献するものと期待できます。
大腸がんは男女ともに発症率が高いがんであり、約5%は単一の病的バリアントの影響により発症すると考えられていました。
しかし多くのデータは海外で実施された研究で収集されており、日本人においてどの遺伝子がどの程度大腸がんの発症に影響しているかは不明でした。
そこで当研究チームでは、疾患群として大腸がんの患者さん約12,000名、
対照群としてがん未発症の方約23,000名を対象として27個の遺伝性腫瘍関連遺伝子を解析し、
MLH1、MSH2、MSH6、APC、BRIP1、BRCA1、BRCA2、TP53遺伝子上の
病的バリアントが発症と関連することを明らかにしました。
また、MLH1、MSH2、MSH6、APC、TP53遺伝子上に
病的バリアントを有する人は早期に大腸がんを発症するという臨床的特徴があり、
がんの家族歴を高頻度で有することを明らかにしました。
悪性リンパ腫には多くの病理組織型が存在しています。 その分類を基にした治療の最適化や病気の予後の予測などを通じて、 悪性リンパ腫の診療は大きく進歩してきました。 過去の研究から、悪性リンパ腫の一部は遺伝的要因が原因と考えられてきましたが、 大規模なゲノム解析データは少なく、遺伝的要因が原因とされる悪性リンパ腫の分類は確立されていません。 そこで当研究チームでは、悪性リンパ腫患者群約2,000名、 がん未発症の方約38,000名を対象として27個の遺伝性腫瘍関連遺伝子について評価しました。 その結果、BRCA1、BRCA2、ATM、TP53の病的バリアントが 悪性リンパ腫の疾患リスクと関連していることが明らかになりました。 更にこれらの病的バリアントは、悪性リンパ腫の病理組織型の一つである マントル細胞リンパ腫の疾患リスクと特に強い関連を認めました。 今後、本研究の情報は悪性リンパ腫のゲノム個別医療体制の構築に貢献するものと期待できます。
ヘリコバクターピロリ(ピロリ菌)感染は、胃がんのリスク因子として広く知られており、
ピロリ菌感染を基盤とする胃がんは東アジアで特に多くなっています。
胃がんのリスク因子としては、ピロリ菌感染という環境要因のほかに、
遺伝要因も知られてきています。
しかし、大規模な症例対照研究を通じた解析が不足していたこともあり、
多くの遺伝子において、臨床でどのような対応が実際に必要かは明らかになっていませんでした。
また、胃がんの発症には遺伝要因と環境要因の双方が影響していますが、
病的バリアントと環境要因を大規模に統合した胃がんのリスク評価はこれまで行われてきていませんでした。
そこで私たちは11,000人以上の胃がん患者と約44,000人以上の非がん対照群を
対象とした愛知県がんセンターとの共同研究を通じて27個の遺伝性腫瘍関連遺伝子を
解析しました。
その結果、APC、ATM、BRCA1、BRCA2、CDH1、
MLH1、MSH2、MSH6、PALB2の病的バリアントが
胃がんの疾患リスクと関連していることが示され、
遺伝子毎の臨床的特徴が明らかとなりました。
更に、相同組換え修復機能関わる遺伝子の病的バリアントが存在すると
ピロリ菌感染による胃がんのリスクがさらに高まることが明らかになり、
病的バリアント保持者は、非保持者と比較して、ピロリ菌除菌により胃がんのリスクを
より一層低減させることができる可能性が示唆されました。
今後、本研究の成果は、診断の精度向上、原因遺伝子を標的とした治療法開発、
より適切な胃がんの予防対策など、胃がんのゲノム医療の構築に寄与するものと
期待できます。
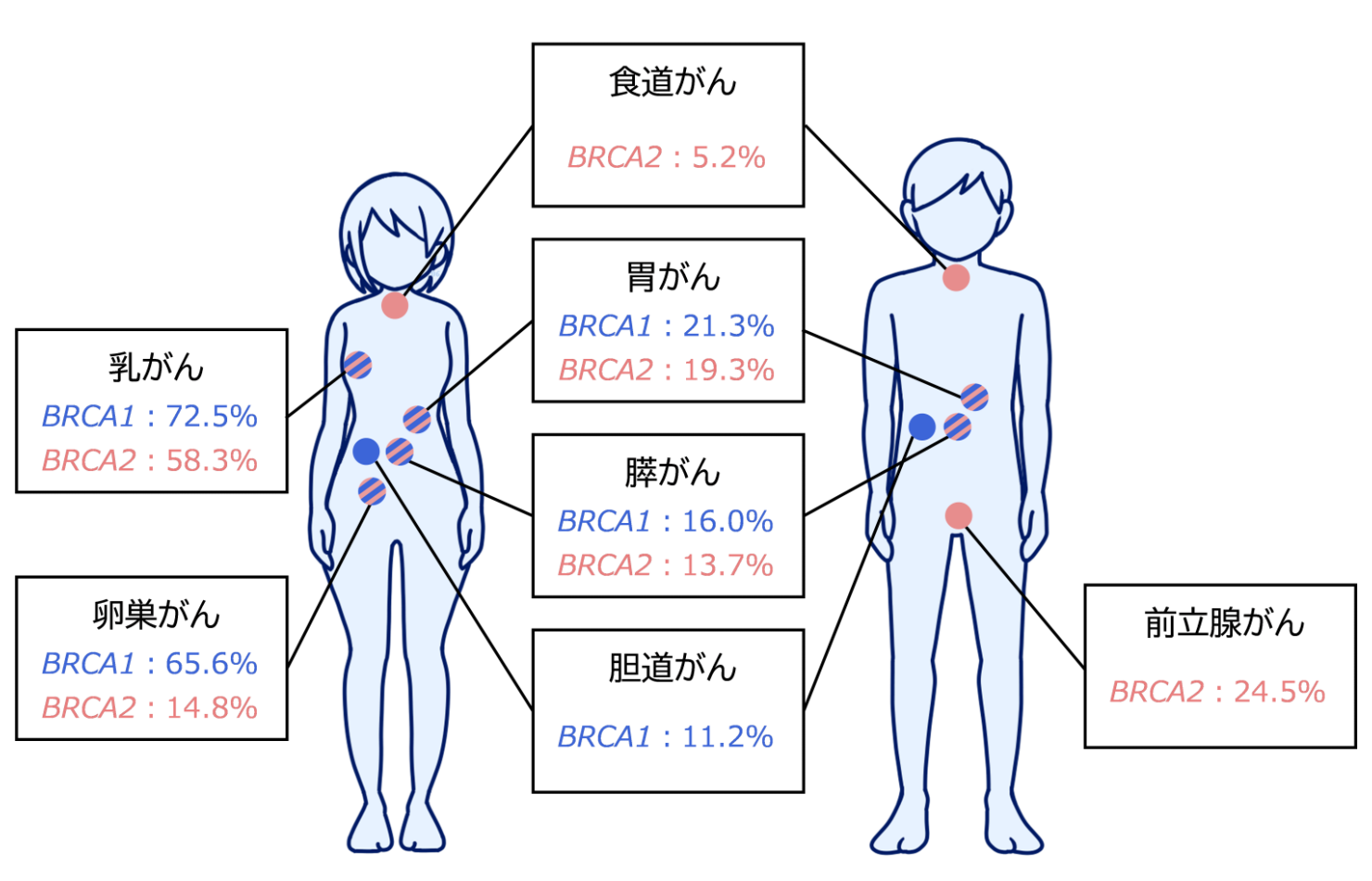
がんは、遺伝と環境の両方の要因により発症すると考えられていますが、一部のがんは1カ所のゲノム配列の違いにより発症リスクが大きく上昇し、 その原因遺伝子としてBRCA1とBRCA2が知られています。 これまで、当研究チームは日本人における遺伝性腫瘍関連遺伝子の病的バリアントを同定し、 乳がん、前立腺がん、膵がん、腎がんのゲノム医療に貢献してきました。 一方で、BRCA1/2遺伝子の病的バリアントは他のがんのリスクも高めることが示唆されています。 そこで、当研究チームは、日本人の14種のがん患者さん約65,000名、対照群として約38,000名を対象にBRCA1/2遺伝子を解析しました。 その結果、既に関連が知られている乳がん、卵巣がん、前立腺がん、膵がんに加えて、 新たに胃がん、食道がん、胆道がんの疾患リスクを高めることを明らかにしました。 その中で、胃がんについては累積リスクも高く、85歳までに20%程度発症することがわかりました。 このことは、関連の知られている4つのがんでBRCA1/2に病的バリアントを持つ患者さんは、 胃がんについても早期スクリーニング検査を行う価値が高いことを示します。 これらの結果は、各がん種において個別化医療が進むものと期待できます。 今後、喫煙・飲酒といった生活習慣など他の要因との解析を行うことで、 より一人ひとりのゲノム情報や生活環境に合わせた個別化医療が可能になると考えられます。
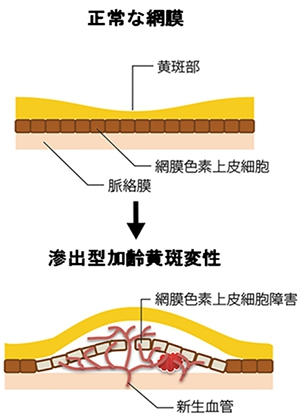
加齢黄斑変性は失明に直結する遺伝性が強い眼科疾患であり、 これまでに原因遺伝子の解明が積極的に行われてきました。 当研究チームでは、2011年に九州大学の研究チームと共同でゲノムワイド関連解析の結果を報告しました ( https://www.riken.jp/press/2011/20110912/ )。 さらに、ゲノムワイド関連解析で疾患との関連が示されたSNPの近傍の遺伝子を対象として、 遺伝子上に存在するレアバリアントの発症への寄与を調査しました。 まず数千個体を対象として標的とする遺伝子領域のみをシークエンスできるターゲットシークエンス法を確立し、 それを疾患群・対照群合計12,223名に適用することで、 CETPおよびCFB遺伝子に存在するレアバリアントが加齢性黄斑変性の発症と関連することを明らかにしました。
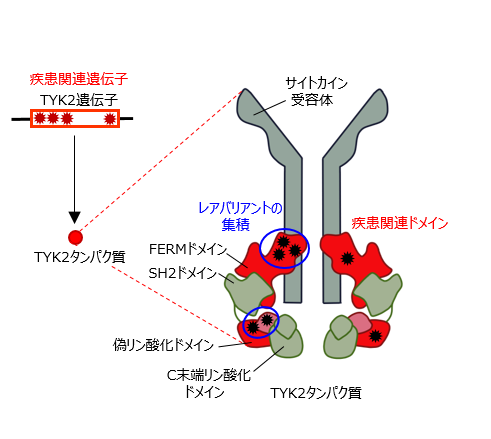
関節リウマチはゲノムワイド関連解析が熱心に行われてきた疾患の一つです。 山本一彦先生が中心となり国際的なメタ解析を実施され、 2014年にはゲノムワイド関連解析後のin silico解析を経て101個の疾患候補遺伝子が明らかになりました ( Nature 506, 376–381 (2014) )。 これらの候補遺伝子から更に遺伝子を絞り込むため、 当研究チームでは疾患群及び対照群合計約6,500名を対象とするシークエンス解析を行い、 TYK2遺伝子上に存在するレアバリアントが発症に寄与することを明らかにしました。 さらに、高地雄太先生のご協力のもと、 当該バリアントが存在する位置によりシグナリングに与える影響が異なることも明らかにしました。
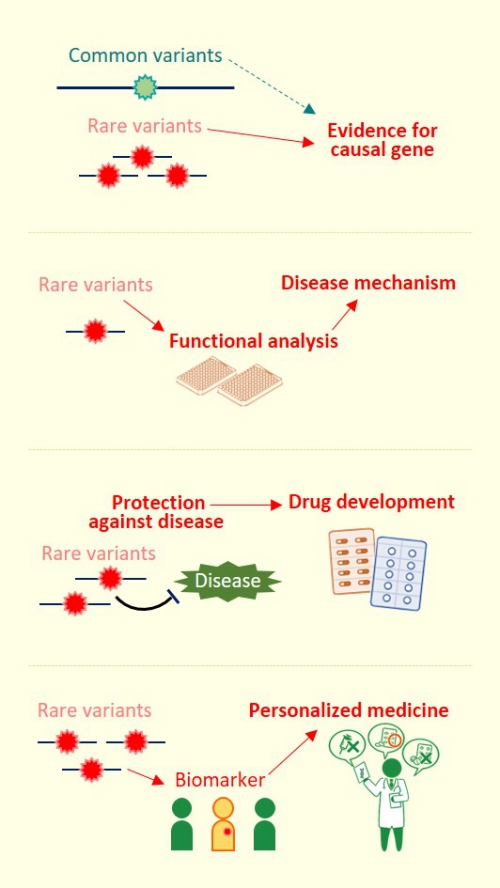
遺伝的バリアントのうち、集団(例えば日本人)における頻度が高いものはコモンバリアント、
低いものはレアバリアントと呼ばれます。
ゲノム医科学研究においては、レアバリアントには特別な役割があると考えています。
その役割として

当研究チームでは、2005年から文部科学省委託事業「オーダーメイド医療実現化プロジェクト」のゲノム解析中核研究機関として、 バイオバンク・ジャパンのサンプルを用いたゲノムワイド関連解析に貢献してきました。 これらの研究成果は日本人における各疾患の遺伝的な側面を明らかにしただけではなく、 国際共同研究による人類共通の疾患メカニズムの探索にも活用されており、 そのデータを利用した研究成果は既に数百にのぼります ( https://biobankjp.org/work/public.html )。 これらのゲノムデータは NBDC に登録されており、許可を得ることで自由に研究に利用できます。 また、対応する臨床データはバイオバンク・ジャパンの試料等利用審査会を経て入手が可能です。
さらに、 日本多施設共同コーホート研究 (J-MICC study) 、 東北メディカル・メガバンク計画 、 多目的コホート研究(JPHC Study) 、 国際薬理遺伝学研究連合 (Global Alliance for Pharmacogenomics: GAP) などの大規模ゲノム解析を担い、共同研究を実施してきました。 また、2020年からは認知症の予防・治療法の開発を目指した 「 健康長寿社会の実現を目指した大規模認知症コホート研究 (JPSC-AD) 」 にも参加しています。 このような大規模ゲノム解析の基盤としての役割は、当研究チームの重要な責務の一つと考えています。

イヌは数万年前にオオカミから家畜化され、 2-300年前には人為選択と少数個体を用いた育種選抜により数百種類の”犬種”が確立されたという歴史を持つ動物です。 以降、遺伝的均質性の高い”犬種”が維持されてきた結果、 ヒトでは稀な疾患が特定犬種で比較的多く認められるようになっています。 このようなイヌという動物の特徴に着目し、 当研究チームではヒトとイヌ共通に罹患する原因遺伝子の同定やメカニズムの解明など、 医療・獣医療の両方に寄与する研究を行っています。
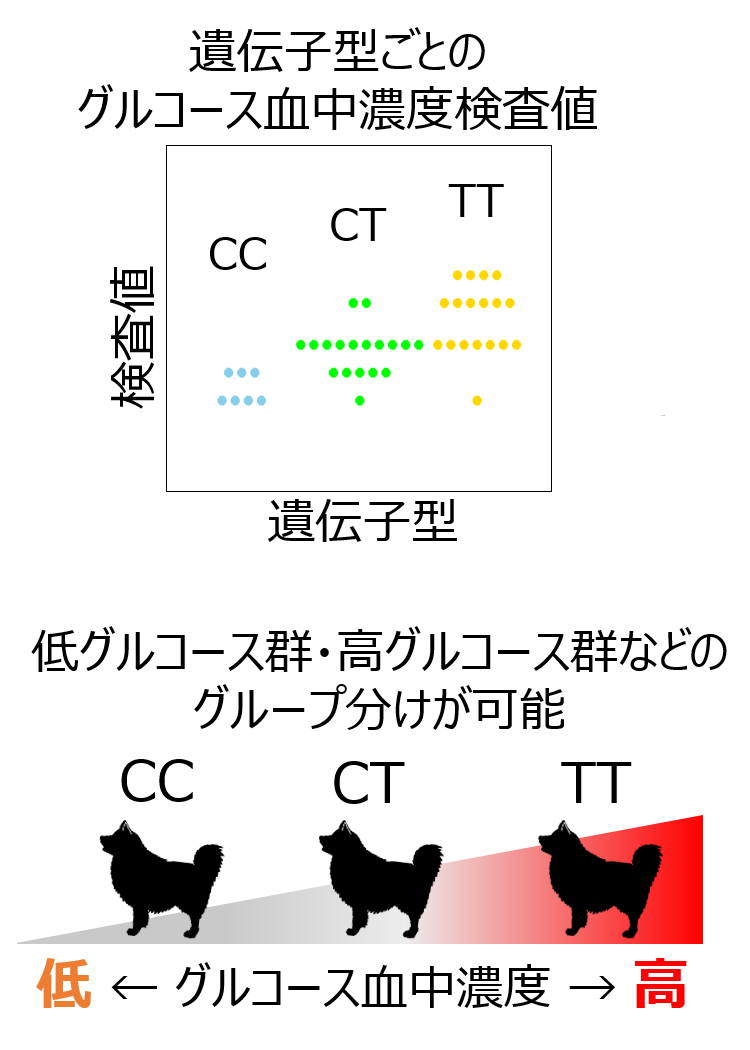
イヌはヒトに比べて遺伝的影響が強いこと、犬種毎に連鎖不平衡の状態が異なることを活かし、 臨床検査値の個体差に関連する遺伝子の同定を試みました。 本研究は、ヨーロッパ12ヶ国による LUPAプロジェクト の一環として実施されました。 8犬種472頭を対象として40種類の検査値についてゲノムワイド関連解析を行った結果、 臨床検査値と関連する13個のバリアントを同定しました。 このうち最も強い関連性が認められたアラニンアミノ基転移酵素(ALT)の個体差へのバリアントの影響は、 ヒトで報告されている数十倍以上と非常に大きいことが明らかとなり、 体の大きさや血中グルコース濃度についても同様の結果が得られました。 本研究より、イヌにおいて遺伝的な影響は臨床判断に及ぼすほど大きいことが明らかになったと共に、 原因の遺伝子を同定する上ではイヌが有用である事が示されました。

東京大学AMED iD3 キャタリストユニットからのご依頼で、 イヌを疾患モデルとした研究によるヒト医療への貢献をまとめたレビューを執筆しました。 現時点の貢献として、ヒトとイヌで共通する疾患の原因遺伝子の同定、単一遺伝子疾患の創薬ターゲットの解明、 ヒトの臨床試験の前段階としてのイヌでの治療効果の評価などが挙げられます。 また、今後犬種毎の遺伝疫学データの集積を進めることにより、ヒトで治療法が見つからない疾患の解消に繋がることが期待されるとまとめました。